10月20日,中国南京天印山医院秦叔逵教授主导的全球随机、开放标签、多中心、3 期临床试验——IMbrave050研究的成果,在线发表于全球医学领域顶级期刊《柳叶刀》(The lancet,IF:168.9)。研究发现,与积极监测相比,根治性手术切除/消融术后使用阿替利珠单抗+贝伐珠单抗辅助治疗可显著改善高复发风险肝细胞癌(HCC)患者的无复发生存(RFS)。该研究为全球首个取得阳性结果的肝癌术后辅助治疗3期研究。

研究背景
目前对于根治性手术切除或消融术后仍有高复发风险的肝细胞癌(HCC)患者,尚无明确的辅助治疗方法。IMbrave050研究旨在评估阿替利珠单抗+贝伐珠单抗(T+A)辅助治疗对比积极监测对高复发风险HCC患者疗效的影响。
研究方法
该研究为一项全球、开放标签、3期临床试验(IMbrave050研究),从WHO的四个地区(欧洲、美洲、东南亚和西太平洋)26个国家的134家医院和医疗中心招募了根治性手术切除或消融术后高复发风险HCC成人患者。患者按1∶1比例随机分组,一组接受阿替利珠单抗(1200mg IV)+贝伐珠单抗(15mg/kg IV)治疗,每3周1次,共17个周期(12个月);另一组接受积极监测。
研究的主要终点是独立审查机构(IRF)评估的意向治疗(ITT)人群的无复发生存(RFS)。
研究结果
ITT人群包括2019年12月31日至2021年11月25日期间随机分组的668例患者,分别接受阿替利珠单抗+贝伐珠单抗治疗(n=334)或积极监测(n=334)。预设的中期分析(2022年10月21日)时,中位随访时间为17.4个月(IQR 13.9~22.1个月)。
与积极监测相比,阿替利珠单抗+贝伐珠单抗辅助治疗显著改善了患者的RFS(HR 0.72,P=0.012)(图1)。
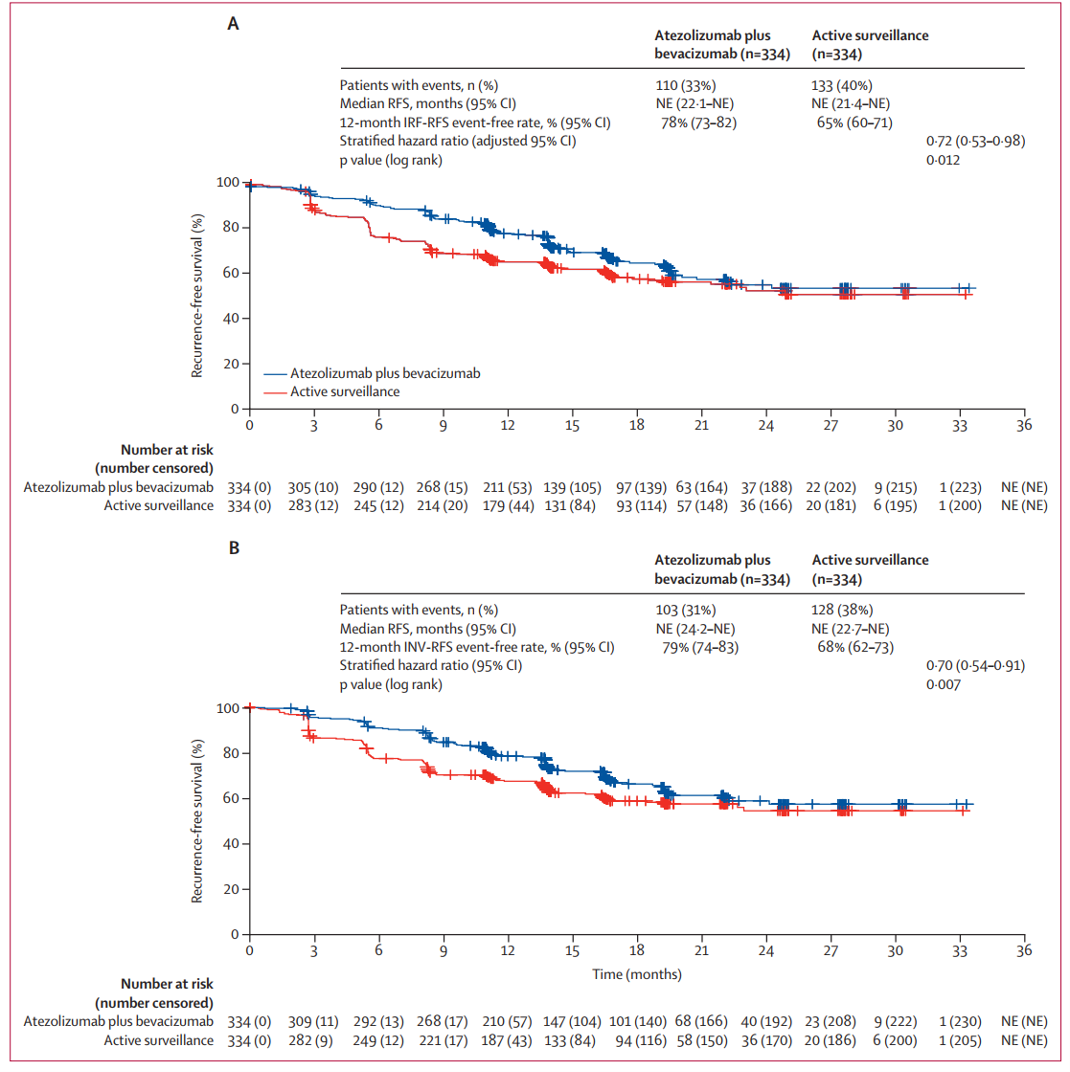
图1 独立审查机构(A)和研究者(B)评估的RFS
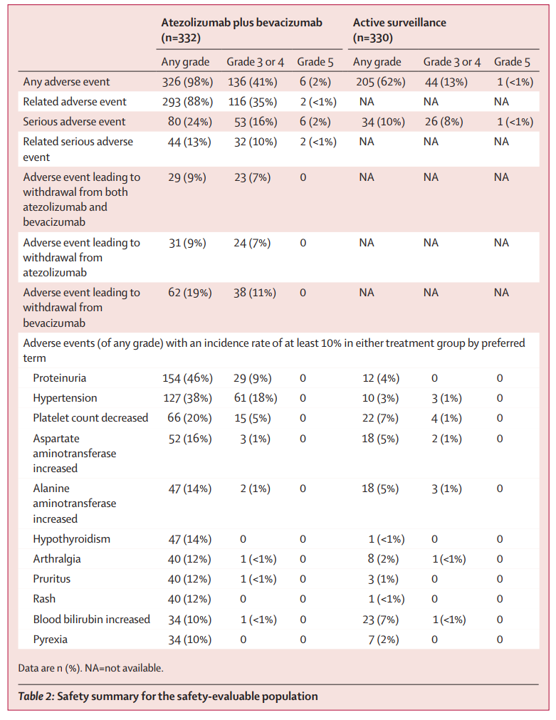
阿替利珠单抗+贝伐珠单抗组和积极监测组分别有41%(136/332例)和13%(44/330例)的患者发生了3-4级不良事件(AE)。两组分别有6例(2%,其中2例与治疗相关)和1例(<1%)患者发生了5级AE(表1)。阿替利珠单抗+贝伐珠单抗组29例(9%)患者因AE停用阿替利珠单抗+贝伐珠单抗治疗。
表1 IMbrave050研究安全性数据
结论
在根治性手术切除/消融术后高复发风险的HCC患者中,与积极监测相比,接受阿替利珠单抗+贝伐珠单抗辅助治疗的患者RFS显著延长。IMbrave050研究是全球首个报告阳性结果的HCC术后辅助治疗3期研究。然而,为了更全面评估获益-风险特征,还需要进行更长时间的随访,包括对无复发生存期(RFS)和总生存期(OS)的观察。