间质-上皮细胞转化因子(MET)是肝细胞生长因子(HGF)的酪氨酸激酶受体,与多种肿瘤的发生发展密切相关。MET基因目前已成为非小细胞肺癌(NSCLC)的重要治疗靶点,MET抑制剂特泊替尼(Tepotinib)已于FDA和NMPA等多个机构中获批适应症,并在NCCN和CSCO等临床指南中被推荐为MET外显子14跳跃突变(METex14跳突)NSCLC患者的首选治疗。MET靶点被认为是肝细胞癌(HCC)的潜在治疗靶点之一,约1%~5%的HCC患者存在MET基因扩增,此类患者或可从MET抑制剂中实现临床获益。近日,中国药科大学附属南京天印山医院秦叔逵教授作为第一作者和通讯作者于Journal of Clinical Oncology刊文整理了特泊替尼应用于MET扩增型HCC的临床前和临床数据,医脉通编辑整理如下。

HCC的靶向治疗进展相对缓慢,尽管针对HCC肿瘤生物标志物的探索从未停止,但迄今为止,尚无可针对性实施靶向治疗且明确带来临床获益的致癌驱动基因获得认可。部分病例报告提示,MET扩增型HCC患者可能从MET抑制剂中获益,因此在多种备受关注的肿瘤标志物中,MET靶点被认为或可成为HCC精准诊疗发展的重要助力。
特泊替尼为METex14跳突型NSCLC患者的生存获益带来了显著改善,基于此,多项临床前研究和探索性临床试验对特泊替尼在HCC中的应用进行了评估,本文汇总了现有的研究数据,以进一步明确特泊替尼在MET扩展型HCC中的治疗获益情况。
共有三项研究评估了特泊替尼在MET扩展型患者来源异种移植(PDX)HCC模型中的临床前获益,均以小鼠作为评估对象。根据研究设计,三项研究可分为两个系列,分别纳入10例和27例HCC PDX模型。研究所纳入的小鼠被随机分配接受特泊替尼100 mg/kg或索拉非尼50 mg/kg或对照性载体治疗,每周第1~5天给药,治疗持续3~5周。研究者每周测量1~2次肿瘤体积变化,以衡量治疗疗效。研究设计如图1所示。
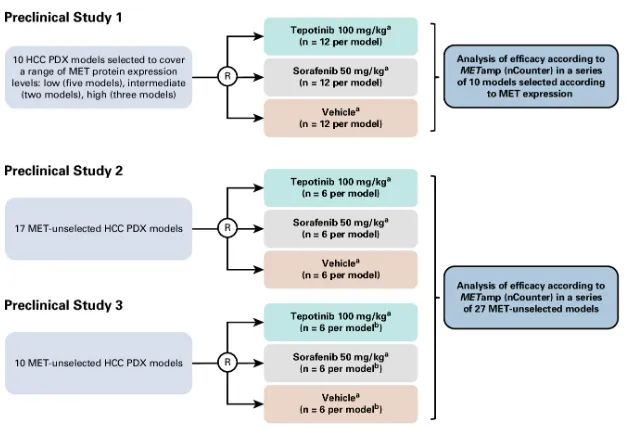
图1 临床前研究设计
DNA分析表明,在系列一的10个模型中,8个的MET扩增水平为无/低,1个的扩增水平为中等(编号:LIM1098),1个的扩增水平为高(编号:LIM612)。针对肿瘤体积变化的分析表明,在接受特泊替尼治疗后,高MET扩增的HCC PDX肿瘤完全缓解,中位肿瘤体积减少达100%;中等MET扩增的HCC PDX中位肿瘤体积增加35%;无/低MET扩增的HCC PDX中位肿瘤体积增加>400%。索拉非尼治疗组未观察到肿瘤消退。如图2所示。
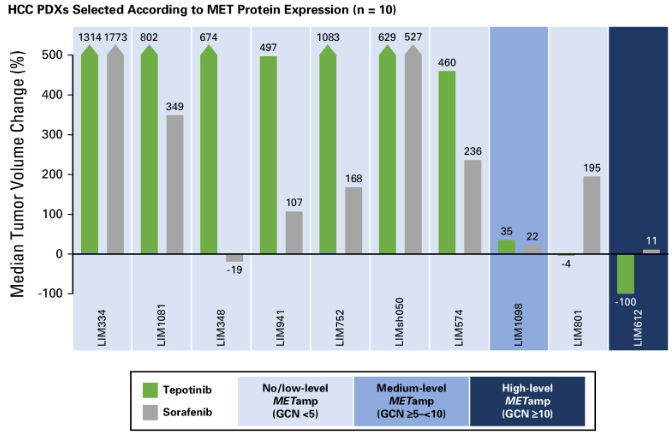
图2 系列一临床前研究结果分析
对于系列二的27个模型,1个的MET扩增水平为高(编号:LIPF210),其余26个均为无/低MET扩增。结果显示,高MET扩增水平的HCC PDX肿瘤几乎完全缓解,中位肿瘤体积减少为99.8%。而无/低MET扩增的HCC PDX中,25个模型的肿瘤体积增加,其中20个>100%。如图3所示。
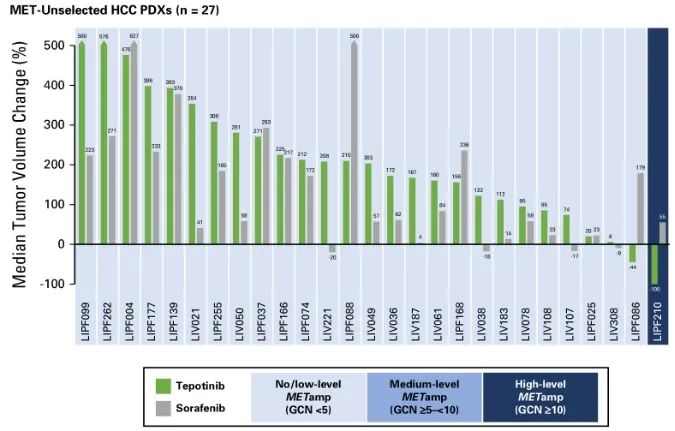
图3 系列二临床前研究结果分析
两项Ib/II期研究评估了特泊替尼在MET扩增型HCC患者中的获益情况。其中一项研究(NCT01988493)旨在探索特泊替尼的一线应用,研究针对亚洲患者开展,Ib期阶段为单臂研究,II期阶段为随机对照研究,治疗组和对照组分别接受特泊替尼500 mg和索拉非尼400 mg的治疗。
另一项研究(NCT02115373)则纳入既往接受索拉非尼治疗的美国/欧洲患者,以单臂的形式探索了特泊替尼的二线应用,研究Ib期阶段所使用特泊替尼的剂量为300 mg或500 mg,最终确定的临床试验二期推荐剂量(RP2D)为500 mg。;两项研究的研究设计如图4所示。
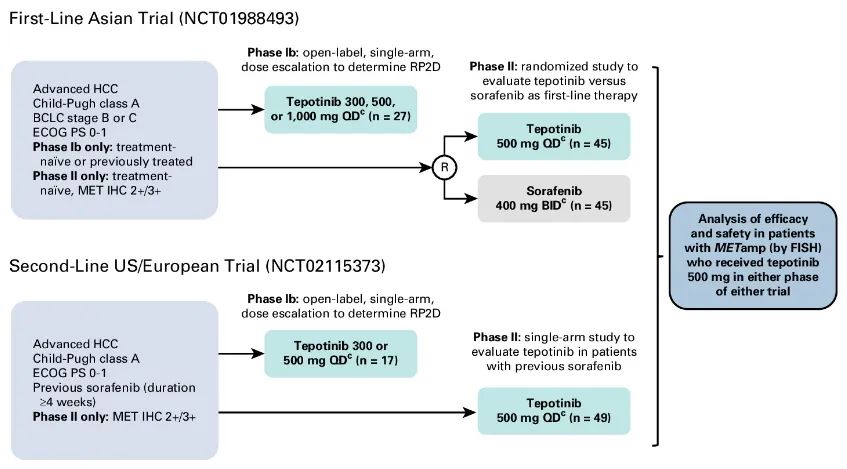
图4 临床研究设计
一项特设分析对上述两项研究的数据进行了汇总,总结了研究者根据RECIST v1.1评估的治疗应答情况、无进展生存期(PFS)、治疗持续时间和治疗相关不良事件(TRAE)。
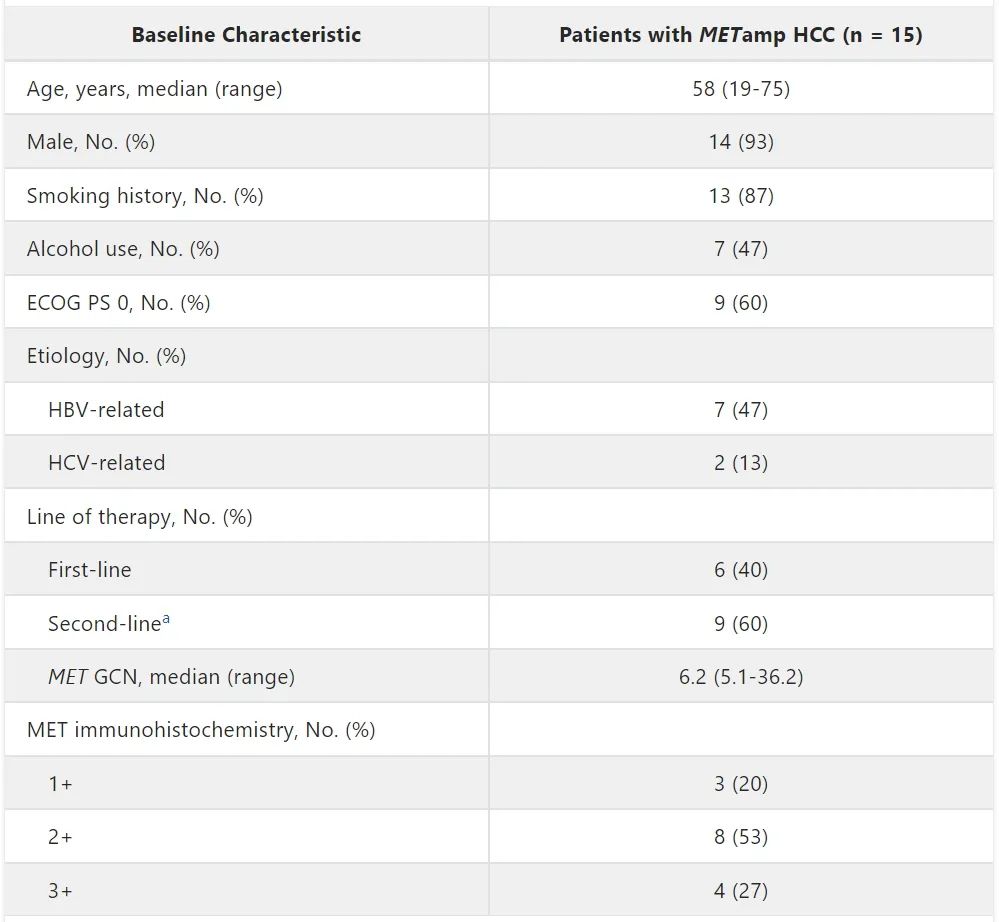
两项研究共纳入121例患者,其中15例存在MET扩增,其中4例患者为高MET扩增水平。6例患者接受特泊替尼一线治疗,其余9例接受二线治疗。15例患者的基线特征如表1所示。
表1 患者基线
分析显示,1例患者实现完全缓解(CR),4例患者实现部分缓解(PR),6例患者为疾病稳定(SD),患者的治疗持续时间、PFS和疾病缓解情况如图5所示。
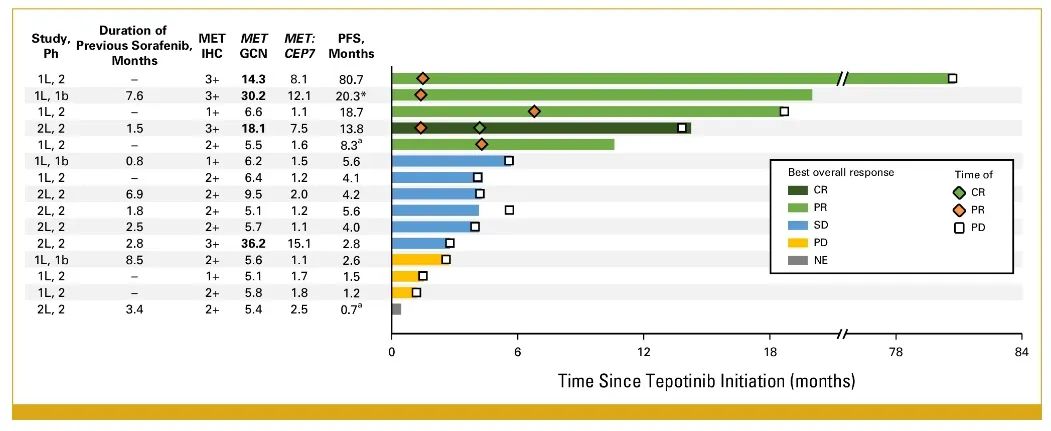
图5 临床研究结果分析
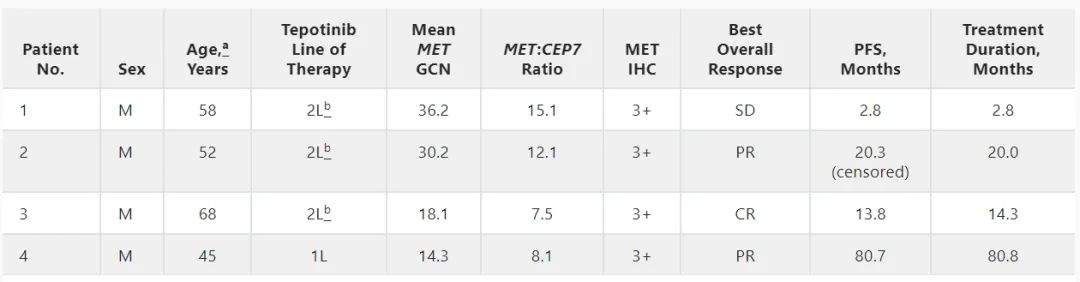
对于4例高MET扩增水平的患者,疾病控制率(DCR)为100%,其中CR和PR分别为1例和2例。3例实现客观缓解的患者治疗持续时间均>12个月,其中1例患者治疗持续时间超过6年。如表2所示。
表2 高MET扩增水平患者结果分析
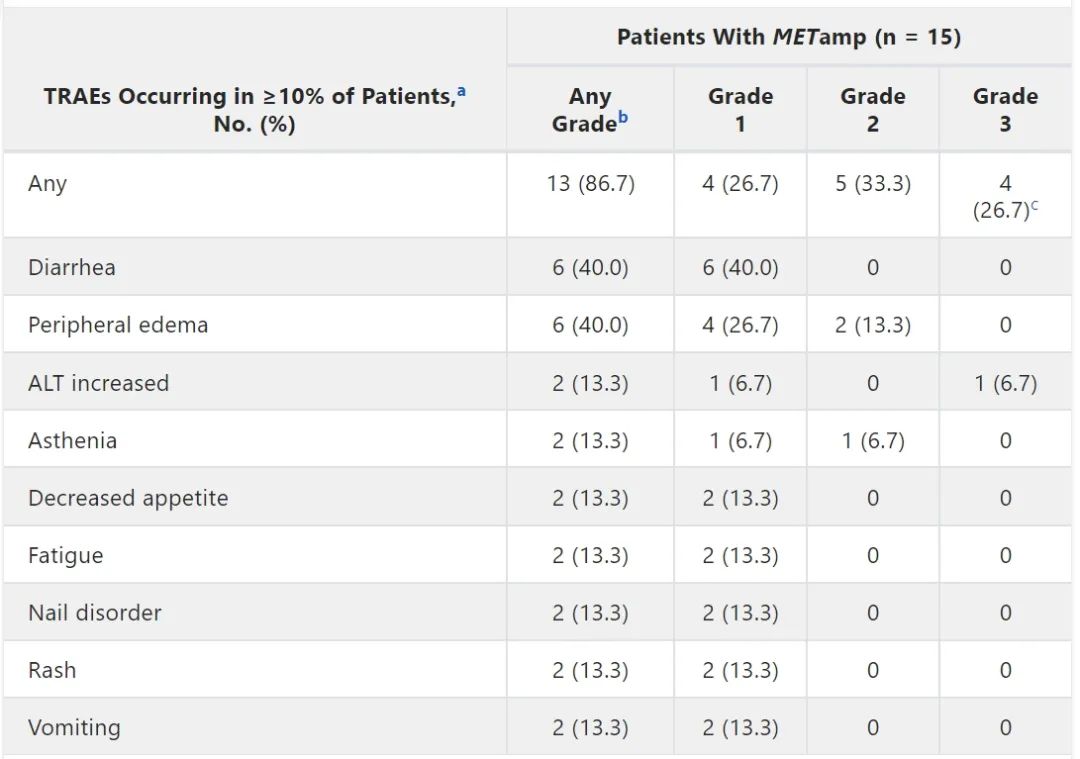
任意级别TRAE的发生率为86.7%,其中最常见的为外周水肿和腹泻。4例患者(26.7%)发生3级TRAE,未发生4/5级TRAE。安全性分析如表3所示。
表3 安全性分析
根据临床前研究,高MET扩增水平是HCC PDX模型对特泊替尼产生应答的重要标志物,特泊替尼在此类模型中的疗效极为可观,可实现近乎100%的肿瘤退缩。而对无/低MET扩增水平的模型,特泊替尼未能产生令人满意的抗肿瘤效果。
两项临床研究进一步证实了这一点,在MET扩增型,特别是高水平MET扩增型HCC患者中,特泊替尼的疗效令人振奋。而且,尽管治疗时间通常较长,但特泊替尼的TRAE多为轻至中度,安全性总体可控。
研究人员认为,尽管研究存在回顾性和样本量较少等限制性因素,但其结果依然为HCC未来的MET靶向治疗发展奠定了基础。特泊替尼在高MET扩增水平HCC PDX模型中展示出了极强的临床前活性,在MET扩增型HCC患者中也显示出良好的临床疗效,研究提示MET扩增水平应被视为HCC的致癌驱动因素,未来应进行大型前瞻性研究以验证上述结果。
参考文献
Qin S, Pan H, Blanc J F, et al. Activity of Tepotinib in Hepatocellular Carcinoma With High-Level MET Amplification: Preclinical and Clinical Evidence[J]. JCO Precision Oncology, 2024, 8: e2300328.